-
18964530232
-
021-54379817

【背景】
自从索尼在1991年实现商业化以来,非水基锂离子电池的众多进展导致了许多产品的出现。为提高能量密度和比能量的努力导致了几十年来对电极活性材料的深入研究。因此,电极活性材料的发展已经远远超过了电解质化学的进展。尽管电解质溶液在电池中作为离子导体在电极之间传输锂离子的关键作用,但今天的电解质溶液的组成与20世纪90年代初基本相同。一个"标准"的电解质配方包含一个线性和环状碳酸酯溶剂的混合物,作为1摩尔(M)的盐溶液,其中的盐通常是六氟磷酸锂(LiPF6)。然后,这种 "标准"电解液主要通过碳酸酯溶剂的变化和添加剂的专有混合物的加入,来适应特定的电池化学特性。这些添加剂可能包括溶剂、盐或其他不被认为是溶剂的分子,与电解质溶剂的量相比,通常使用的量很小。最近,Solchenbach等人建议,添加剂与活性材料的比例可能比特定浓度更相关。然而,任何特定添加剂的理想用量可能取决于其在电池中的功能,以及在不对影响性能的其他特性产生重大负面影响的情况下获得所需效果的用量。添加剂在电池中实现了许多目的,如用于形成固体电解质界面(SEI)、阴极电极界面(CEI)的成膜剂(即牺牲性添加剂)或提高系统安全性的化合物(如阻燃剂)。作为一个例子,CEI添加剂的用量可能较低,以避免增加界面电阻,而不是如阻燃剂的用量,其中需要较高的含量以影响自熄灭时间。
就主要的电解质溶液成分而言,仍然有一个相当大的竞争领域,只是在最近几年才开始被探索(图1)。例如,不含碳酸乙烯酯(EC)的电解质的概念已经被探索出来,以提高高压应用。盐的浓度方面是一个特别值得探索的方面。浓度的变化直接影响到Li+离子在溶液中的溶解,随后影响到所有其他电解质的特性,包括界面层(SEI和CEI)的形成。
图1:电解质及其性能与对电池的影响。
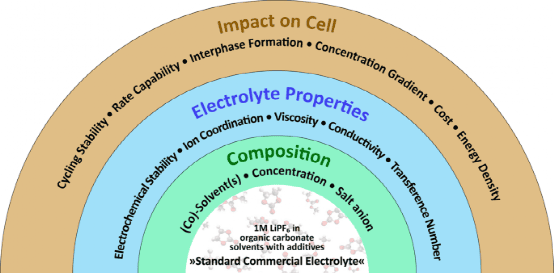
在图的中间,描述了标准的商业锂离子电池电解质溶液。这种标准电解液不仅可以通过改变成分(如溶剂或盐的阴离子),还可以通过改变浓度来改变(绿色环)。成分的变化会影响电解质的特性(蓝环),随后影响电池的性能(橙环)。
充足的锂离子传输特性对于令人满意地保证电化学储能性能是必要的。传统的智慧(即电池电解质溶液领域的专家普遍接受的对电解质特性的理解和解释)说是通过高导电性和低粘度的电解质实现的。在大多数非水锂离子导电电解质溶液中,最大的体电导率出现在大约1M的盐浓度。因此,"标准"电解质浓度为1M并非巧合。Borodin等人将此称为 "1摩尔(M)特性"。这种最大的电导率是由电荷载流子的数量和这些电荷载流子的离子迁移率之间的权衡结果。电荷载体的数量由盐的解离决定,而离子流动性主要与电解质介质的粘性有关。在1M浓度体系中,锂离子被 "传统使用的 "碳酸酯溶剂溶解,而阴离子基本上被认为是 "自由"的(通常被称为溶剂分离的离子对或SSIP)。溶剂化壳的结构,即锂离子和直接配位的电解质成分,取决于溶剂和盐阴离子的性质。此外,还有大量的非配位溶剂,即第一溶剂化壳之外的溶剂分子。在高盐浓度下,锂离子的配位情况非常不同。锂离子同时被阴离子和溶剂分子配位。此外,自由溶剂分子很少(如果有的话),它们不仅影响电解质的传输特性,而且还影响电解质和电池中其他成分之间的相互作用,例如在SEI/CEI形成中。
对 "1M "和 "高盐浓度"电解质溶液的比较导致了一个问题,什么是"高浓度"?不幸的是,这个问题没有单一的答案,因为非水电池电解质溶液的不同浓度制度之间的界限高度依赖于定义标准。从描述电解质行为的几乎所有经典方程都来自于表意的角度来看,溶液中的所有离子必须完全解离,参与扩散和迁移,并且独立移动(即不受其他离子的影响)。然而,电池电解质溶液在浓度低于0.1M时就已经偏离了理想状态;因此,即使是 "标准"的1M电解质溶液也可以被视为浓缩电解质。因此,"浓缩电解质 "的实际定义与基于独立离子运动的理想定义有很大不同。
最近有人提出,将实用电解质(即技术上相关的电化学储能装置中使用的电解质)划分为浓度制度的一种方法可能是基于离子溶剂化壳的性质。如上所述,在高浓度电解质(或 "超浓缩 "电解质)中,很少(如果有的话)有自由溶剂分子,阴离子存在于第一溶剂化壳中。相反,在 "低浓度 "电解质中(即基于上述摩尔值定义的小于3M),有溶剂分子没有直接与溶液中的阳离子配位,因此是自由的。
上面的浓度是以摩尔值(即每升溶液中溶质的摩尔数)给出的,这在文献中经常使用。然而,对于高浓度的电解质溶液来说,摩尔值不一定是衡量浓度的最佳标准,因为密度会随着浓度的变化而显著变化。作为一个例子,含有双(氟磺酰)亚胺锂(LiFSI)的电解质在EC中的密度从0.63M时的1.38g cm-3增加到5.67M时的1.71g cm-3。因此,表达浓度的其他单位,如molality(即每1公斤溶剂中溶质的摩尔数)或摩尔比(摩尔溶质:摩尔溶剂),更适合,特别是在广泛的浓度范围内比较电解质。
作为上面提到的传统智慧的延伸,当体电导率较低且粘度增加时,预计高浓度电解质的电池性能会更差。这一假设主要来自于低浓度时的情况,在低浓度时,车辆运输机制(即锂离子在电解质中的溶剂化壳移动)对锂离子的传导性有很大贡献。在这种情况下,"较低的浓度 "取决于溶剂,可以认为碳酸酯的浓度高达约3M。对高浓度电解质溶液的研究结果的考察,导致了对这种传统智慧的质疑,因此,作为关键评估标准的电解质电导率的有用性。其他传输机制,如结构扩散,即锂离子通过第一溶剂化壳中的成分交换(即离子耦合-解离过程),是否也能有效地将 "足够的 "锂传输到电极上?高浓度的锂离子能否将电解质中浓度梯度的影响降到最低?基于这两个问题,是否需要改变对传输特性和电池性能之间联系的传统理解模式?此外,个别电解质成分的电化学稳定性是否可以通过配位来改变,配位是如何影响界面的形成?
体电导率或锂迁移数作为关键传输特性的比较
体电解质电导率(材料的内在离子电导率,不受任何界面的影响,例如,由于在多孔结构中的限制)经常被用作评估电解质在电池测试前的关键传输特性。离子电导率是一个可以用大多数电化学实验室中的标准设备相对容易和可靠地进行筛选的参数。尽管如此,还是有一定的局限性;最值得注意的是,高的电解质电导率并不一定意味着高锂离子电导率。
锂离子传输对总电流的贡献被称为锂的迁移数。迁移数的概念并不是液体锂离子电解质溶液所特有的。它是一个一般的概念,用来描述特定物种x对总(即体)电导率的贡献(x的迁移数,Tx,值在0和1之间)。在 "标准"电解质系统中,该值通常较低(在0.2和0.4之间),这意味着"自由"阴离子比具有溶剂溶剂化壳的锂离子更具流动性。因此,阴离子,例如PF6--上面定义的 "标准"电解质,对整个电流贡献更大。在一个特定的电解质中,锂离子的电导率σLi+,可以从大量电解质电导率σ和TLi+的乘积中确定(即σLi+= σ∙TLi+)。最终,是锂离子电导率限制了在电化学电池中使用特定电解质所能达到的电流密度。
对高浓度电解质的研究表明,与低浓度电解质相比,具有较低体电导率的电解质溶液可以改善电化学储能性能。这个最初反直觉的结果意味着具有较低体电导率的电解质必须具有较高的锂离子电导率,这表明较高的TLi+。当同行评议的报告中给出TLi+值时,高浓度电解质中的TLi+值高于更稀的"标准"电解质溶液(例如:1M LiPF6 in EC/DMC(体积比为3:7)TLi+ = 0.42;4M LiTFSI + 0.5M LiDFOB in FEC/DMC TLi+ = 0.58;1M LiPF6 in EC/DMC(体积比为1:2)TLi+ = 0.32;[LiFSI]:[乙腈]:[碳酸乙烯酯] = 0.52:1:0.0917 TLi+ = 0.57)。
由于在电解质内形成较低的浓度梯度,较高的锂离子电导率导致电极上锂离子的可用性较高。最近的一项研究使用原位拉曼光谱检查了施加电流后电池中固定位置的电解质中的锂离子数量。高浓度的电解质溶液(即10M)形成的浓度梯度明显较低。一项进一步的研究表明,尽管粘度和离子传导性是低质量负荷(如0.95 mAh cm-2)和薄电极(如22微米)的锂离子电池的良好性能指标,但更高浓度的电解质(如1.9 M)可以缓解厚电极(如8.10 mAh cm-2质量负载和161微米厚)的孔隙中锂离子的消耗,以提高电化学储能性能。值得注意的是,体电解质溶液的离子传导性通常高于限制在电极或隔膜的多孔结构中的电解质。
使用从迁移数得出的锂离子电导率作为预测电解质溶液行为的关键传输参数会有好处。然而,在准确测量迁移数方面存在相当大的挑战。在电化学方法(如Bruce-Vincent方法)和脉冲场梯度核磁共振获得的结果中存在着明显的差异。每种方法都有特定的限制/假设,必须加以考虑。因此,迁移数不可能作为一个通用的筛选工具。然而,迁移的概念及其对电池单元中锂离子浓度梯度的影响应该在关注电解质的研究工作中加以考虑。
对粘度影响
电解质溶液中的高盐浓度是以高粘度为代价的,这大大阻碍了离子的流动性。如上所述,高浓度下的溶剂量已不足以完全填充第一溶剂化壳。因此,阴离子参与了锂离子配位。溶剂量不足也会导致阴离子与一个以上的锂离子配位,形成通常所说的 "聚合体 "的情况。聚合体的形成与阴离子配位一起有效地增加了溶解的锂离子的离子半径。由于流动性与粘度和离子半径的乘积成反比,两者在高浓度时都较大,结果是锂基复合物的流动性大大降低。这一结果与带电粒子在电场中运动所感受到的力(电和拖)的经典图片是一致的,并描述了基于车辆运输机制的离子运动。然而,研究表明,当聚合体存在时,结构扩散对整体运输的贡献是很大(图2A),因此可以帮助抵消高粘性的其他影响。
图2:开发高浓度电解质溶液需要考虑的方面。
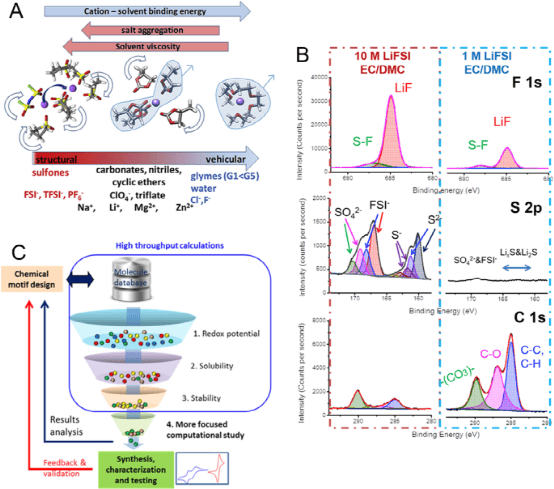
A 影响液态电解质中金属阳离子的车辆和结构扩散运输机制的参数。B在浓缩(10M)和标准(1M)LiFSI的EC:DMC(体积比为1:1)电解质溶液中循环的金属锂的XPS分析。C 使用高通量计算的关键特性筛选候选材料,以进行重点计算研究和/或合成和测试。
电解液粘度不仅在锂离子传输特性方面起作用,而且在对电池生产和形成很重要的方面也起作用,即电解液填充和润湿(尽管具体电解液的润湿性,如接触角所定义的,可能起更关键的作用)。例如,已经表明,使用高粘度离子液体为基础的电解质溶液的实验室规模的电池的容量在最初的循环中随着电极逐渐被电解质润湿而增加。可以使用各种策略来理解和缓解缓慢的润湿。例如,可以将作为 "稀释剂 "的溶剂加入到高浓度电解质溶液中,这些溶剂不改变局部传输机制和溶化结构,但会降低粘度。这个概念相对较新,被描述为局部高浓度电解质(LHCE),似乎很有希望。除了改性电解质,分析方法可以用来更好地理解和跟踪润湿。例如,中子射线照相术已被用来估计润湿程度,而超声波传播已被提议作为在线监测工具。
不同的浓度,不同的界面
除了传输特性,电解液的电化学稳定性和界面的形成是获得令人满意的电池性能的关键方面。在 "标准"商业电解质中,SEI/CEI的形成主要是由添加剂和电解质溶剂驱动的,这些添加剂和溶剂存在过量,而且基本上不与锂离子配位。在高浓度下,电解质的电化学稳定性以及由此产生的界面性会受到各种因素的影响,例如,第一溶剂化壳中阴离子的存在和大部分溶剂的锂配位。在这种情况下,"高浓度 "不能缩小到一个特定的浓度范围,而应该根据配位来定义,如上文所述。最近一篇同行评议的文章详细描述了在锂基非水电解质溶液中阳离子、阴离子和溶剂之间发生的复杂相互作用。几项研究的一个有趣的结果是阴离子配位和界面组成之间的联系。界面的性质从主要由溶剂及其分解产物主导转变为主要由阴离子及其分解产物影响,包括LiF(图2B)。鉴于盐对高浓度电解质的界面的重要性,探索LiPF6以外的其他盐,并研究所形成的SEI/CEI的特性当然是很有趣的。LiFSI在这方面已经获得了兴趣。其他选择包括使用双盐系统或特定的辅助溶剂(如LHCEs)。使用盐和/或溶剂的混合物的方法允许利用各种电解质成分的优势来解决其他电池成分可能出现的问题(例如,正极的铝集流体的腐蚀)。
下一代锂基电池的电解质的发展
推动高浓度电解质研究的因素之一是希望使电池能够充分利用高电压的阴极材料和锂金属阳极。可能需要高容量或高电压的电极材料来补偿由于高浓度电解质的密度增加而造成的能量含量(特别是比能量)的损失。即使高浓度电解质已经与石墨阳极一起使用(并且通常与高压阴极配对),专注于锂金属电极的工作肯定在文献报道中占主导地位。
锂金属阳极的主要挑战之一是需要控制沉积形态,以避免锂金属的苔藓状或树枝状生长。在这方面,高浓度的电解质溶液比 "标准"电解质显示出明显的优势。一些研究表明,高浓度电解质(或也是LHCEs)能够在电流密度为1 mA cm-2时,以更密集和圆形的沉积锂形态来沉积金属锂。在类似的条件下,"标准"的1M碳酸酯基电解质溶液中得到了枝晶结构。在这些例子中,作者将改进的金属锂沉积(和溶解)行为归因于来自浓缩电解质的SEI的组成变化(其中SEI也取决于所调查的电解质溶液的组成)。
除了这里讨论的非水电解质外,其他非常规电解质,如盐水电解质(WISE)或混合水基非水电解质(HANE),最近也越来越受到关注。WISE和HANE利用完全的溶剂配位(如上面定义的高浓度电解质)来扩展其他非锂基储能技术中水电解质的典型电化学稳定性窗口。然而,仍然需要进行大量的研究,以使这些系统能够与非水电解质竞争,用于锂基电池。
新型电解质成分和配方的进一步发展可以从涉及高通量和自主测试平台与机器学习相结合的新研究方法中受益。对特定性质的计算筛选可以限制进行深入研究的分子数量(图2C)。由机器学习算法指导的自主平台可用于优化配方,可能导致具有独特性质的非直观电解质成分,这一点已经在水电解质溶液中得到证明。此外,使用先进的表征技术可以更好地了解电解质在电池运行过程中的表现。作为一个例子,原位拉曼表征允许直接调查电解质中的锂离子耗竭情况。考虑到电解质在电池中的多方面作用及其在性能和寿命方面的影响,创新的研究方法与先进的分析方法的结合将很可能被证明是特别重要。
成本将最终成为实施高浓度电解质的一个驱动因素。尽管感兴趣的主要盐类的成本只有相对较小的差异,但电解质溶剂和盐类的成本之间有一个~10的系数。因此,减少溶剂的用量和增加盐的用量会导致电解质配方成本的净增加。正如最近文献所指出的那样。重要的是,"成本 "并不总是金钱上的,也可以是技术上的,特别是在考虑将新的组件整合到现有的电池生产过程中。
在今天的锂离子电池的生产过程中,化成和老化步骤是时间和金钱方面最昂贵的步骤。因此,节省这一生产步骤将是有益的。虽然已知在高浓度电解质中,界面的性质和组成会发生变化,但在电池生产过程中,对形成步骤的潜在影响(从时间和相关的货币成本来看)仍然是未知的。成本问题比来自材料本身的问题要复杂得多。因此,高浓度电解质溶液的性能的好处可能必须是显著的,以超过目前 "标准"1M电解质溶液的成本。
在可预见的未来,"标准"1M电解质溶液可能仍然是当前一代锂离子电池的最新技术。然而,使用高浓度电解质溶液获得的令人鼓舞的实验结果有可能为未来的高电压和高能量锂基电池开辟一条替代途径。尽管大量的离子电导率仍将是一个可获得的、可靠的和具有成本效益的电解质开发筛选工具,但重要的是要记住,最高的电导率并不一定能带来 "最好的"电池性能,特别是在速率能力方面。抛开传统的电解质智慧,专注于锂离子电导率(迁移数)和电解质内浓度梯度的形成(导致锂离子耗竭)等方面,可能会激发使用高于标准1M浓度的电解质研究的新途径。然而,不能忘记了解界面化学的重要性,因为高浓度电解质的使用改变了科学家对界面形成的许多认识。
The role of concentration in electrolyte solutions for non-aqueous lithium-based batteries
Nature Communications ( IF 17.694 ) Pub Date : 2022-09-06 , DOI: 10.1038/s41467-022-32794-z
Guinevere A. Giffin(弗劳恩霍夫陶瓷技术和系统研究所)
申明:如本站文章或转稿涉及版权等问题,请您及时联系本站,我们会尽快处理!